Định luật bảo toàn khối lượng là nội dung quan trọng trong chương trình Hóa học, giúp các bạn học sinh dễ dàng giải quyết các bài tập tính toán hóa học. Bài viết sau đây Monkey sẽ tổng hợp chi tiết lý thuyết về chủ đề này để các bạn theo dõi.
.png)
|
XEM VIDEO TỔNG QUAN BÀI VIẾT |
Định luật bảo toàn khối lượng là gì?
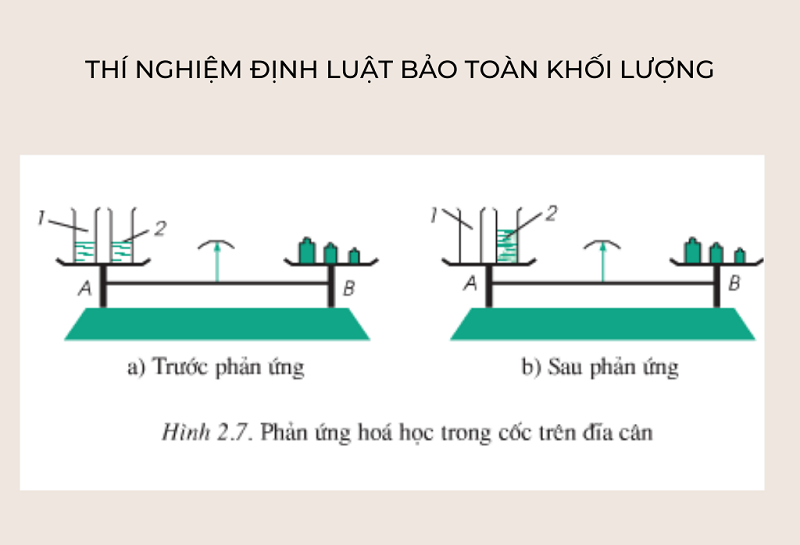
Trước khi đi tìm hiểu cụ thể nội dung định luật bảo toàn khối lượng là gì, chúng ta hãy cùng suy nghĩ lại thí nghiệm về định luật này. Cụ thể thí nghiệm như sau:
-
Trên đĩa cân số I đặt 2 cốc thí nghiệm (1) chưa bari clorua (BaCl2) và (2) chứa dung dịch natri sunfat (Na2SO4).
-
Đặt quả cân lên đĩa II cho đến khi cân bằng.
-
Đổ cốc (1) vào cốc số (2) sau đó lắc cho 2 dung dịch hòa lẫn vào nhau. Quan sát cốc đó ta thấy có chất rắn màu trắng, không tan xuất hiện được gọi là BaSO4.
Quan sát thí nghiệm ta thấy: Kim của chiếc cân vẫn không thay đổi và giữ nguyên như ban đầu. Điều này chứng tỏ rằng, khi có một phản ứng hóa học xảy ra thì tổng khối lượng các chất sẽ không có sự thay đổi.
Phát biểu nội dung định luật bảo toàn khối lượng theo SGK Hoá Học 8: “Trong một phản ứng hóa học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng” (Sách giáo khoa Hóa học, Nhà Xuất bản Giáo dục Việt Nam).
Định luật bảo toàn khối lượng do ai phát hiện ra? Giải thích định luật bảo toàn khối lượng
Định luật bảo toàn khối lượng do 2 nhà khoa học Lô-mô-nô-xốp (1711- 1765) người Nga và La-voa-diê (1743 – 1794) người Pháp tiến hành độc lập và phát hiện ra.
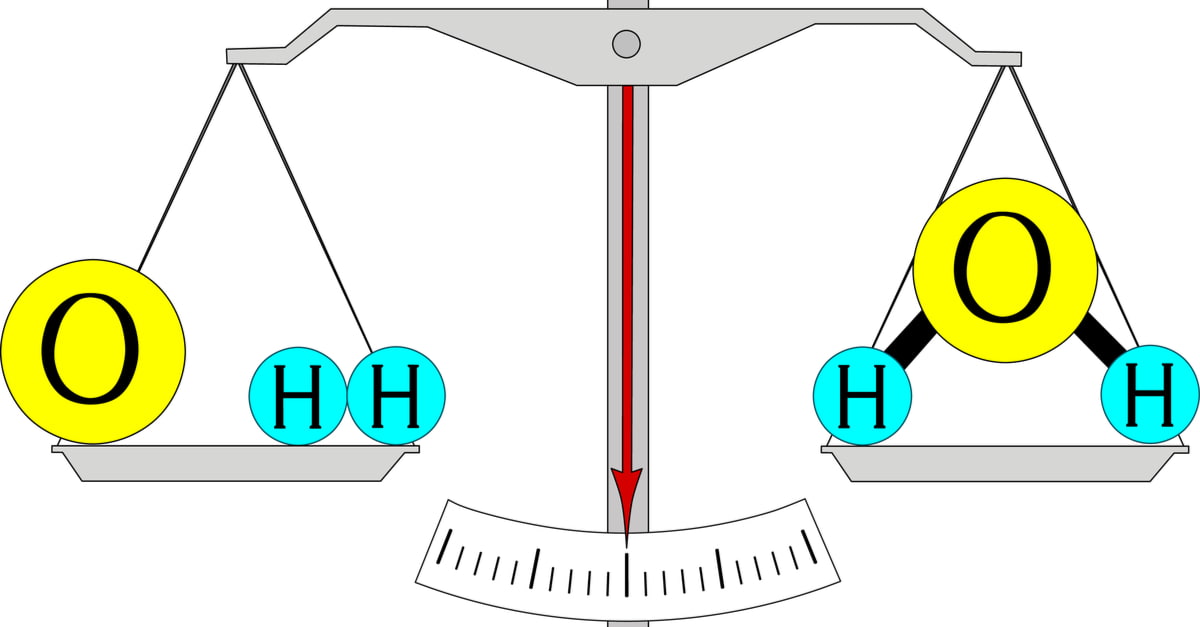
Sau khi nêu định nghĩa định luật bảo toàn khối lượng, nội dung quan trọng tiếp theo chúng ta cần làm là giải thích về định luật này. Thực tế, trong phản ứng hóa học diễn ra sự thay đổi liên kết giữa các nguyên tử. Sự thay đổi này chỉ liên quan đến các electron. Chính bởi vậy, số nguyên tử mỗi nguyên tố giữ nguyên và khối lượng của các nguyên tử không đổi. Cho nên, tổng khối lượng các chất sẽ được bảo toàn.
Ý nghĩa của định luật bảo toàn khối lượng
Định luật bảo toàn khối lượng cho chúng ta biết trong mỗi phản ứng hóa học chỉ có sự thay đổi liên quan đến electron, còn số nguyên tử của nguyên tố vẫn giữ nguyên cũng như khối lượng của các nguyên tử không đổi. Bởi vậy, khối lượng của các chất được bảo toàn.
Phương trình bảo toàn khối lượng trong hoá học
Để áp dụng định luật bảo toàn khối lượng, ta viết nội dung định luật này thành công thức. Giả sử rằng có phản ứng giữa 2 chất A và B sẽ tạo ra chất C và D. Lúc này, công thức định luật bảo toàn khối lượng lớp 8 được viết như sau: mA + mB = mC + mD.
Trong đó:
- mA là khối lượng của chất A
- mB là khối lượng của chất B;
- mC là khối lượng của chất C
- mD là khối lượng của chất D.
Ví dụ về công thức trên là: Khối lượng BaCl2 + Khối lượng Na2SO4 = Khối lượng BaSO4 + Khối lượng NaCl.
Khi viết được khối lượng của 3 chất ta sẽ dễ dàng tính được khối lượng của chất còn lại.

Áp dụng định luật như sau: “Trong một phản ứng có n chất, kể cả chất phản ứng và sản phẩm, nếu biết khối lượng của (n-1) chất thì tính được khối lượng của chất còn lại” (Sách Giáo khoa Hóa học 8, NXB Giáo dục Việt Nam).
Bài tập định luật bảo toàn khối lượng
Một số bài tập thực hành về định luật bảo toàn khối lượng dưới đây sẽ giúp bạn nắm vững kiến thức lý thuyết nội dung định luật bảo toàn khối lượng và áp dụng tính khối lượng chất dễ dàng trong một phản ứng hóa học.
Bài tập định luật bảo toàn Hóa học 1
Phát biểu định luật bảo toàn khối lượng và giải thích tại sao khi một phản ứng hóa học xảy ra khối lượng được bảo toàn.
Trả lời:
Nội dung định luật bảo toàn khối lượng được định nghĩa như sau: “Trong một phản ứng hóa học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng”.
Giải thích: Một phản ứng hóa học xảy ra khối lượng được bảo toàn vì trong phản ứng hóa học, sự thay đổi chỉ liên quan đến electron, nguyên tử được bảo toàn, không mất đi.
Bài tập định luật bảo toàn Hóa học 2
Đốt cháy hết 9g kim loại magie (Mg) trong không khí thu được 15g hợp chất magie oxit MgO. Biết rằng magie cháy là phản ứng với khí oxi O2 trong không khí.
Trả lời:
Ta có công thức: mMg + mO2 = mMgO
mO2= mMgO – mMg = 15 - 9 = 6(g).
|
XÂY DỰNG NỀN TẢNG TOÁN HỌC VỮNG CHẮC CHO TRẺ TỪ NHỎ VỚI ĐA PHƯƠNG PHÁP DẠY HỌC TÍCH CỰC, CHI PHÍ CỰC RẺ CHƯA ĐẾN 2K/NGÀY CÙNG MONKEY MATH.  |
Bài tập về định luật bào toàn khối lượng tự luyện
Ngoài những bài tập trong sách giáo khoa, dưới đây là một số bài tập thêm để các em có thể tự luyện để hiểu rõ kiến thức này hơn:
Bài 1:
a. Phát biểu chính xác định luật bảo toàn khối lượng.
b. Hãy giải thích vì sao khi một phản ứng hóa học xảy ra, khối lượng các chất được bảo toàn?
Bài 2:
Trong phản ứng hóa học như sau: Bari clorua + Natri sunphat tạo ra bari sunphat + natri clorua. Cho biết khối lượng của natri sunphat Na2SO4 là 14,2 gam, còn khối lượng của bari sunphat BaSO4 và khối lượng natri clorua NaCl lần lượt là : 23,3 g và 11,7 g.
Bạn hãy tính khối lượng của bari clorua BaCl2 đã tham gia phản ứng.
Bài 3:
Đem đốt cháy hết 9g kim loại magie Mg trong không khí, ta thu được 15g hỗn hợp chất magie oxit MgO. Biết rằng magie cháy sẽ xảy ra phản ứng với oxi O2 ở trong không khí.
a. Hãy viết phản ứng hóa học trên.
b. Hãy viết công thức về khối lượng của phản ứng xảy ra ở trên.
c. Hãy tính khối lượng của khí oxi đã tham gia phản ứng.
Bài 4:
Đem đốt cháy m(g) cacbon cần 16g oxi, ta thu được 22g khí cacbonic. Bạn hãy tính m.
Bài 5:
Đem đốt cháy 3,2g lưu huỳnh S ở trong không khí, ta thu được 6,4g lưu huỳnh đioxit. Bạn hãy tính khối lượng của oxi đã tham gia phản ứng.
Bài 6:
Ta đem đốt cháy m(g) kim loại magie Mg ở trong không khí, ta thu được 8g hợp chất magie oxit (MgO). Biết rằng khối lượng magie Mg khi tham gia bằng 1,5 lần khối lượng của oxi (không khí) tham gia phản ứng.
a. Bạn hãy viết phản ứng hóa học.
b. Hãy tính khối lượng của Mg và oxi đã tham gia phản ứng.
Bài 7:
Đá đôlomit (đây là hỗn hợp của CaCO3 và MgCO3), khi nung nóng đá này tạo ra 2 oxit là canxi oxit CaO, magie oxit MgO và thu được khí cacbon đioxit.
a. Hãy viết phản ứng hóa học xảy ra, cũng như phương trình khối lượng nung đá đolomit.
b. Nếu như nung đá đôlomit, sau phản ứng thu được 88 kg khí cacbon đioxit và 104 kg hai oxit các loại thì phải ta phải dùng khối lượng đá đôlomit là bao nhiêu?
A. 150kg B. 16kg C. 192kg D. Kết quả khác
Bài 8:
Bạn hãy giải thích vì sao khi ta nung thanh sắt thì thấy khối lượng của thanh sắt tăng lên. Còn khi nung nóng đá vôi lại thấy khối lượng bị giảm đi?
Bài 9:
Khi hòa tan cacbua canxi (CaC2) vào nước (H2O) ta thu được khí axetylen (C2H2) và canxi hiđroxit (Ca(OH)2).a. Hãy lập phương trình khối lượng cho phản ứng trên. b. Nếu như ta dùng 41g CaC2 thì thu được 13 g C2H2 và 37 g Ca(OH)2. Vậy cần phải dùng bao nhiêu mililit nước cho phản ứng trên? Biết rằng khối lượng riêng của nước là 1g/ml.
Bài 10:
Khi cho Mg tác dụng với axit clohiđric thì khối lượng của magie clorua (MgCl2) nhỏ hơn tổng khối lượng của Mg và axit clohiđric khi tham gia phản ứng. Vậy, điều này có phù hợp với định luật bảo toàn khối lượng hay không? Bạn hãy giải thích.
FAQ - Một số câu hỏi thường gặp
1. Định luật bảo toàn khối lượng là gì?
Định luật bảo toàn khối lượng phát biểu rằng: Trong một phản ứng hóa học, tổng khối lượng các chất tham gia phản ứng bằng tổng khối lượng các chất tạo thành.
2. Ai là người phát hiện ra định luật bảo toàn khối lượng?
Định luật do M.V. Lomonosov và sau đó được A. Lavoisier chứng minh và hoàn thiện.
3. Định luật bảo toàn khối lượng áp dụng trong trường hợp nào?
Áp dụng cho các phản ứng hóa học xảy ra trong hệ kín, không có chất thoát ra hoặc xâm nhập từ bên ngoài.
4. Định luật bảo toàn khối lượng có áp dụng cho phản ứng hạt nhân không?
Không. Trong phản ứng hạt nhân, khối lượng có thể chuyển hóa thành năng lượng (theo ).
5. Định luật này giúp ích gì trong học tập hóa học?
Giúp cân bằng phương trình hóa học và tính toán khối lượng các chất trong phản ứng.
6. Khi phản ứng có chất khí thoát ra thì định luật còn đúng không?
Vẫn đúng nếu xét toàn bộ hệ kín (bao gồm cả chất khí thoát ra).
7. Có thể áp dụng định luật này trong đời sống không?
Có. Ví dụ như nấu ăn, đốt nhiên liệu, quá trình lên men đều tuân theo nguyên lý bảo toàn khối lượng.
8. Vì sao cần học định luật bảo toàn khối lượng?
Vì đây là định luật nền tảng của hóa học, giúp hiểu bản chất phản ứng và làm tốt các bài toán hóa học.
Bài học về định luật bảo toàn khối lượng không khó, chỉ cần chú tâm là các bạn có thể dễ dàng nắm bắt nội dung chủ đề này. Rất nhiều chia sẻ hữu ích về kiến thức môn học sẽ được Monkey gửi tới các bạn qua chuyên mục này, hãy đón đợi các bài viết tiếp theo của chúng tôi nhé.









.png)
.png)



![[Thảo luận] Giai đoạn chuyển tiếp ở trẻ | Kỷ luật tích cực #19](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:22:39_giai-doan-chuyen-tiep-o-tre-ky-luat-tich-cuc.png)
![[Thảo luận] Tác hại khi phạt trẻ bằng đòn roi | Kỷ luật tích cực #18](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:16:33_tac-hai-khi-phat-tre-bang-don-roi-ky-luat-tich-cuc.png)
![[Thảo luận] Cơn thịnh nộ (ăn vạ) của trẻ | Kỷ luật tích cực #17](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:04:28_con-thinh-no-va-an-va-cua-tre-ky-luat-tich-cuc.png)


.png)