Muối cacbonat phân chia thành nhiều loại khác nhau với những tính chất và ứng dụng cụ thể. Cùng Monkey tìm hiểu chi tiết về loại muối này và giải các bài tập trong SGK qua bài viết dưới đây.
.png)
Khái niệm muối cacbonat là gì?
Muối cacbonat là muối của axit cacbonic, nó gồm 2 loại nhỏ là muối cacbonat CO32- và hidrocacbonat HCO3-. Muối cacbonat rất phổ biến và có nhiều ứng dụng trong cuộc sống như làm nguyên liệu sản xuất vôi, xi măng, xà phòng, thuốc chữa bệnh…

Phân loại muối cacbonat
Muối cacbonat được phân loại thành 2 loại chính bao gồm cacbonat trung hòa và cacbonat axit.
-
Muối cacbonat trung hòa: Được gọi là muối cacbonat, không còn nguyên tố H trong thành phần gốc axit. Ví dụ như: Magie cacbonat (MgCO3), canxi cacbonat (CaCO3), natri cacbonat (Na2CO3)…
-
Muối cacbonat axit: Được gọi là muối hidrocacbonat, nghĩa là chúng có nguyên tố H trong thành phần gốc axit. Ví dụ như natri hidrocacbonat NaHCO3; canxi hidrocacbonat (Ca(HCO3)2, kali hidrocacbonat (KHCO3)…
Tính tan của muối cacbonat
Đa phần, các muối cacbonat không tan trong nước, trừ một số muối cacbonat của kim loại kiềm như Na2CO3, K2CO3… Ngược lại, hầu hết muối hidrocacbonat tan trong nước ví dụ như Mg(HCO3)2, Ca(HCO3)2…
Tính chất hóa học của muối cacbonat
Muối cacbonat có những tính chất hóa học điển hình như tác dụng với dung dịch axit mạnh, tác dụng với dung dịch bazơ, tác dụng với dung muối, dễ bị nhiệt phân hủy giải phóng khí CO2 (trừ Na2CO3, K2CO3…). Cụ thể:

Muối cacbonat tác dụng với axit
Muối cacbonat có khả năng tác dụng với axit mạnh hơn axit cacbonic tạo thành muối mới và giải phóng khí CO2.
Để chứng minh cho tính chất hóa học này của muối cacbonat, SGK Hóa học 9 đã nêu thí nghiệm cụ thể cho dung dịch NaHCO3 và Na2CO3 lần lượt tác dụng với dung dịch axit clohidric (HCl). Quan sát thí nghiệm ta thấy có hiện tượng bọt khí thoát ra ở cả 2 ống nghiệm. Điều này xảy ra do phản ứng hóa học:
NaHCO3 (dd) + HCl (dd) -> NaCl (dd) + H2O (l) + CO2 (k)
Na2CO3 (dd) + 2HCl (dd) -> 2NaCl (dd) + H2O(l) + CO2 (k)
Tác dụng với dung dịch bazơ
Một số dung dịch muối cacbonat phản ứng với dung dịch bazơ tạo thành muối cacbonat không tan và bazơ mới
Ví dụ:
K2CO3 (dd) + Ca(OH)2 (dd) -> CaCO3 (rắn – trắng) + 2KOH (dd)
Lưu ý: Muối hidrocacbonat tác dụng với dung dịch kiềm sẽ tạo thành muối trung hòa và nước.
Ví dụ:
NaHCO3 (dd) + NaOH (dd) -> Na2CO3 (dd) + H2O (l)
Tác dụng với dung dịch muối
Dung dịch muối cacbonat có thể tác dụng với một số dung dịch muối khác, kết quả tạo ra 2 muối mới.
Ví dụ: Thực hiện thí nghiệm cho dung dịch natri cacbonat (Na2CO3) tác dụng với dung dịch canxi clorua (CaCl2) thấy có hiện tượng vẩn đục hoặc kết tủa trắng xuất hiện. Ta có phương trình phản ứng như sau:
Na2CO3 (dd) + CaCl2 (dd) -> CaCO3 (rắn – trắng) + 2NaCl (dd)
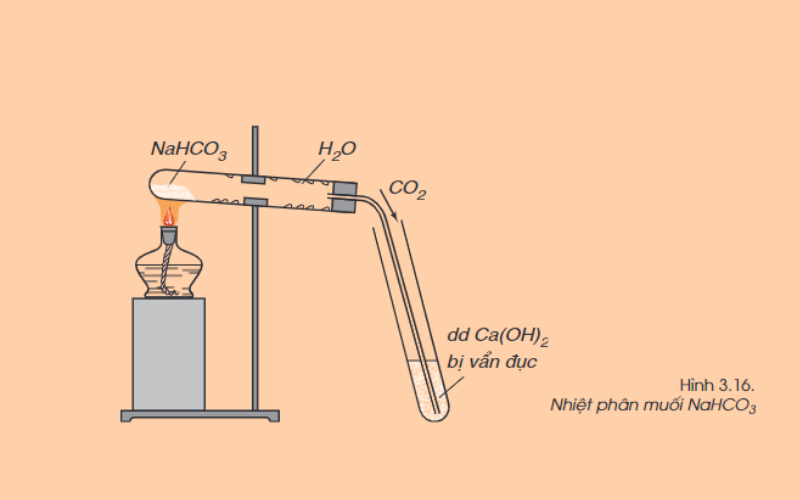
Phản ứng phân hủy muối cacbonat
Nhiều muối cacbonat, trừ muối cacbonat trung hòa của kim loại kiềm rất dễ bị nhiệt phân hủy giải phóng khí cacbonic. Ví dụ:
CaCO3 (r) -> nhiệt độ CaO (r) + CO2 (k)
2NaHCO3 (r) -> nhiệt độ Na2CO3 (r) + H2O (h) + CO2 (k)
Xem thêm:
- Muối là gì? Tổng hợp kiến thức từ A-Z và bài tập thực hành
- Muối kali nitrat (KNO3): Định nghĩa, tính chất, cách điều chế và ứng dụng
- Cacbon oxit (CO) là gì? Tính chất và các ứng dụng phổ biến
Ứng dụng muối cacbonat trong đời sống và sản xuất
Muối cacbonat có nhiều ứng dụng trong đời sống thực tiễn cũng như trong sản xuất công nghiệp. Mỗi muối cacbonat cụ thể lại có những ứng dụng riêng:

|
Tên muối |
Ứng dụng |
|
CaCO3 (canxi cacbonat) |
Ứng dụng trong công nghiệp xây dựng như cẩm thạch, đá xây dựng, thành phần cấu thành của xi măng. Ứng dụng trong ngành sơn, canxi cacbonat được sử dụng như chất độn chính. Ứng dụng làm tấm trần, khung nhựa, ống PVC… |
|
Na2CO3 (natri cacbonat) |
Nguyên liệu sản xuất thủy tinh (chiếm 13-15%) Làm chất phụ gia trong xà phòng, chất tẩy rửa. Nguyên liệu cho nhiều sản phẩm hóa chất gốc natri. |
|
NaHCO3 (natri bicarbonat - baking soda) |
Tạo độ giòn, xốp và làm đẹp cho bánh. Tạo bọt và tăng PH trong một số loại thuốc như thuốc nhức đầu. Giải quyết các vấn đề răng miệng như phòng ngừa sâu răng, mòn răng, bệnh nha chu… Ứng dụng làm các chế phẩm trung hòa acid dịch vị chữa bệnh trào ngược dạ dày… |
Bài tập về muối cacbonat SGK Hóa học 9 kèm lời giải
Một số bài tập về muối cacbonat để các bạn ôn tập lại kiến thức lý thuyết và áp dụng thực hành:

Bài tập 2 SGK Hóa học 9, trang 91
Dựa vào tính chất hóa học của muối cacbonat, hãy nêu tính chất của muối MgCO3 và viết các phương trình hóa học minh họa.
Gợi ý đáp án:
MgCO3 có tính chất của muối cacbonat.
-
Tác dụng với dung dịch axit:
MgCO3 + H2SO4 → MgSO4 + CO2 ↑ + H2O.
-
MgCO3 không tan trong nước, không tác dụng với dung dịch muối và dung dịch bazơ.
-
Dễ bị phân hủy:
MgCO3 -> (nhiệt độ) MgO + CO2.
Bài tập 3 SGK Hóa học 9, trang 91
Viết các phương trình hóa học biểu diễn chuyển hóa sau:
C -> CO2 -> CaCO3 -> CO2
Gợi ý đáp án:
Các phương trình hóa học:
(1) C + O2 ->(nhiệt độ) CO2
(2) CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
(3) CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Bài tập 4 SGK Hóa học 9, trang 91
Hãy cho biết trong các cặp chất sau đây, cặp nào có thể tác dụng với nhau.
a) H2SO4 và KHCO3; b) K2CO3 và NaCl; c) MgCO3 và HCl; d) CaCl2 và Na2CO3; e) Ba(OH)2 và K2CO3
Giải thích và viết các phương trình hóa học.
Gợi ý đáp án:
Những cặp chất tác dụng với nhau là cặp chất a, c, d và e. Phương trình hóa học như sau:
H2SO4 + 2KHCO3 → K2SO4 + 2CO2 ↑ + 2H2O
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
CaCl2 + Na2CO3 → CaCO3 ↓ + 2NaCl
Ba(OH)2 + K2CO3 → BaCO3 ↓ + 2KOH
Cặp chất không tác dụng với nhau: b).
Lưu ý: Điều kiện của phản ứng trao đổi trong dung dịch chỉ xảy ra nếu sản phẩm có chất kết tủa (không tan) hoặc có chất khí tạo thành.
Bài tập 5 SGK Hóa học 9, trang 91
Hãy tính thể tích khí CO2 (đktc) tạo thành để dập tắt đám cháy nếu trong bình chữa cháy có dung dịch chứa 980g H2SO4 tác dụng hết với dung dịch NaHCO3.
Gợi ý đáp án:
Phương trình hóa học của phản ứng:
2NaHCO3 + H2SO4 → Na2SO4 + 2CO2 ↑ + 2H2O
Như vậy: nCO2 = 2 x nH2SO4 = 10 x 2 = 20 mol.
VCO2 = n x 22,4 = 20 x 22,4 = 448 lít.
Trên đây là tổng quan toàn bộ kiến thức lý thuyết về muối cacbonat và gợi ý lời giải một số bài tập trong SGK để bạn đọc ôn tập. Hãy ghé đọc website Monkey thường xuyên để tham khảo thêm nhiều kiến thức môn học thú vị và đừng quên chia sẻ nếu thấy bài viết hữu ích bạn nhé!










.png)
.png)

![[Thảo luận] Giai đoạn chuyển tiếp ở trẻ | Kỷ luật tích cực #19](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:22:39_giai-doan-chuyen-tiep-o-tre-ky-luat-tich-cuc.png)
![[Thảo luận] Tác hại khi phạt trẻ bằng đòn roi | Kỷ luật tích cực #18](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:16:33_tac-hai-khi-phat-tre-bang-don-roi-ky-luat-tich-cuc.png)
![[Thảo luận] Cơn thịnh nộ (ăn vạ) của trẻ | Kỷ luật tích cực #17](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:04:28_con-thinh-no-va-an-va-cua-tre-ky-luat-tich-cuc.png)


.png)