HCl có ứng dụng quan trọng trong các ngành công nghiệp xử lý nước, sản xuất thực phẩm, sản xuất sắt thép… Vậy HCl là gì, tính chất của nó có gì đặc biệt? Cùng Monkey tìm hiểu nội dung bài giảng về hidro clorua, axit clohidric và muối clorua trong bài viết dưới đây.
.png)
Khái niệm HCl là gì?
HCl là công thức chung của khí hiđro clorua và axit clohidric. Trong đó:
.jpg)
-
Hidro Clorua HCl
- Khái niệm: Hiđro Clorua là chất khí không màu, có mùi xốc, tan nhiều trong nước (1 lít nước có thể hòa tan 500 lít HCl ở 20 độ C).
- Cấu tạo phân tử: H – Cl. Hidro Clorua là một hợp chất cộng hóa trị, phân tử có cực.
-
Axit clohiđric HCl
Hidroclorua HCl tan trong nước tạo thành axit mạnh - Axit clohidric HCl
- Khái niệm: Axit clohiđric HCL là chất lỏng không màu, có mùi sốc, nồng độ đặc nhất tới 37%.
- Hiện tượng Axit clohidric “ bốc khói” trong không khí ẩm, nguyên nhân là do hiđro clorua thoát ra cùng với hơi nước trong không khí tạo thành nhiều hạt dung dịch nhỏ như sương mù.
Tìm hiểu về hidro clorua
Để nghiên cứu độ tan của khí HCl trong nước, người ta tiến hành thí nghiệm: Đưa khí HCl vào đầy bình ống nghiệm, đậy bình bằng nút cao su. Xuyên một ống thuỷ tinh thẳng, nhọn qua nút cao su. Ông thuỷ tinh được nhúng vào chậu nước có pha quỳ tím.
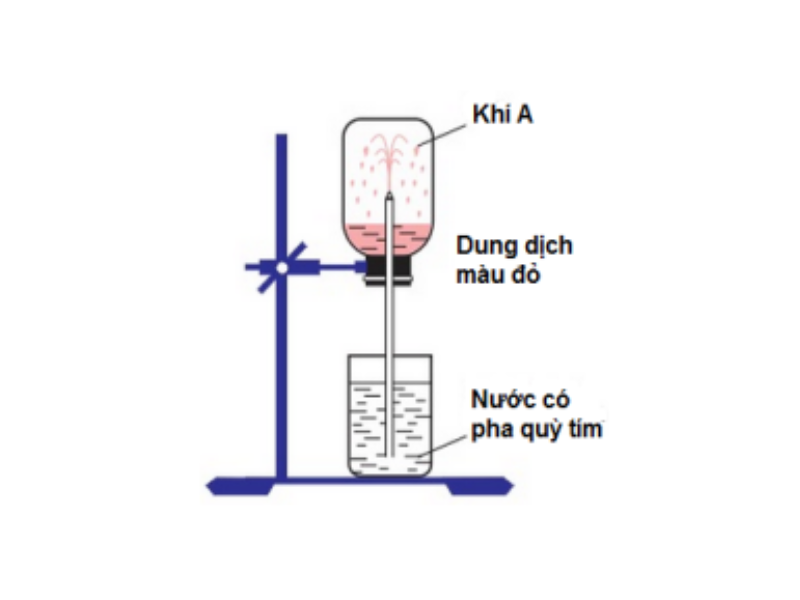
Người ta quan sát thấy hiện tượng: Nước trong chậu theo ống phun xuất hiện những tia nước màu đỏ. Giải thích điều này, khí hiđro clorua tan nhiều trong nước, khiến áp suất trong bình giảm mạnh, áp suất của khí quyển đẩy nước vào thay thế chỗ khí HCl đã hoà tan.
.jpg)
Như vậy, ta có kết luận về Hidro clorua như sau:
-
Khí HCl tan rất nhiều trong nước.
-
Khí HCl nặng hơn không khí (d= 36.5/29)
-
Khí HCl không làm quỳ tím chuyển đỏ. Dung dịch thu được là axit clohidric mới có khả năng làm quỳ chuyển đỏ.
-
Khí HCl không phản ứng với CaCO3.
Tìm hiểu chi tiết về axit clohidric HCl
Ở phần này, chúng ta cùng tìm hiểu chi tiết hơn về dung dịch axit clohidric HCl.

Tính chất vật lý của axit clohidric
Dưới đây là 4 tính chất vật lý điển hình của axit clohidric mà bạn cần nhớ:
-
Axit clohidric là dung dịch không màu, có mùi xốc.
-
Dung dịch HCl đạt đến mức đặc nhất ở nồng độ C% = 37% (ở 20 độ C)
-
Dung dịch HCL hòa tan trong nước, D = 1.19(g/ml).
-
Dung dịch HCL đặc bốc khói trong khí ẩm.
Tính chất hóa học của axit clohidric
Axit clohidric là một axit mạnh, mang đầy đủ tính chất của một axit với các phản ứng:
-
Axit clohidric HCl làm quỳ tím chuyển đỏ.
-
Axit clohidric HCl tác dụng với kim loại trước H, tạo ra muối. Trong đó, kim loại có hóa trị thấp + H2.
Ví dụ: Fe + 2HCl → FeCl2 + H2 (bay hơi)
Lưu ý: Pb đứng trước H nhưng không tan trong dung dịch HCl.
-
Axit clohidric HCl tác dụng với oxit kim loại tạo ra muối. Trong đó, kim loại giữ nguyên hóa trị + H2O.
Ví dụ: Fe3O4 + 8HCl → 4H2O + FeCl2 + 2FeCl3
-
Axit clohidric HCl tác dụng với bazơ tạo ra muối. Trong đó, kim loại giữ nguyên hóa trị + H2O.
Ví dụ: Fe(OH)2 + 2HCl → FeCl2 + 2H2O
-
Axit clohidric HCl tác dụng với muối tạo ra muối mới + axit mới.
Ví dụ: Na2CO3 + 2HCl → 2NaBr + H2O + CO2
Bên cạnh là một axit mạnh, HCl còn thể hiện tính oxi hóa khử:
-
Tính oxi hóa: HCL thể hiện tính oxi hóa khi kết hợp với các kim loại trước H.
-
Tính khử: Tính khử này có được là do trong phân tử HCl, Clo có số oxi hóa thấp nhất là -1. Khi dung dịch HCl đặc tác dụng với các chất oxi hóa mạnh như: KMnO4, K2Cr2O7, MnO2, KClO3, ... thì HCl bị oxi hóa thành Cl2 theo phương trình:
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
(+4) (-1) (+2) (0)
Điều chế axit clohidric như thế nào?
Điều chế axit clohidric như thế nào? Cùng tìm hiểu 2 phương pháp điều chế HCl phổ biến: Trong công nghiệp và trong phòng thí nghiệm.
Điều chế axit clohidric HCl trong phòng thí nghiệm
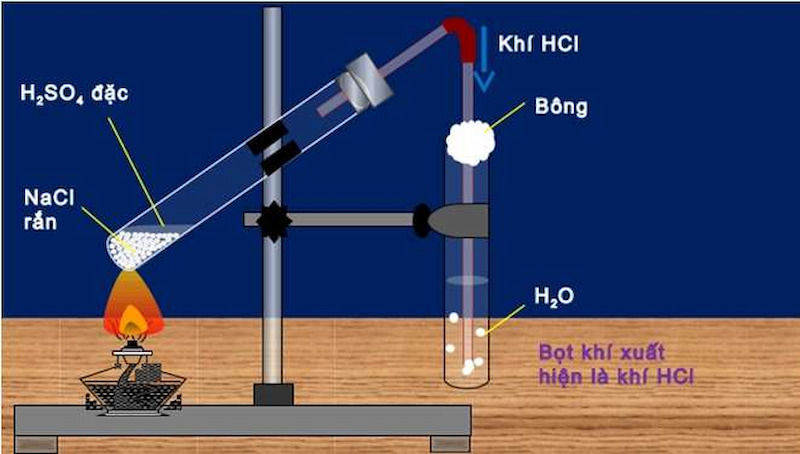
Trong phòng thí nghiệm, người ta điều chế HCl bằng phương pháp sunfat - cho tinh thể NaCl tác dụng với H2SO4 đặc và đun nóng, sau đó hấp thụ vào nước.
Phương trình phản ứng như sau:
NaCl + H2SO4 → NaHSO4 + HCl (nhiệt độ < 250 độ C)
2NaCl + H2SO4 → Na2SO4 + 2HCl (nhiệt độ từ 400 độ C trở lên)
Sản xuất axit clohiđric trong công nghiệp
Trong công nghiệp, HCl được điều chế bằng cách đốt cháy H2 trong khí quyển Cl2. Trong đó cả 2 chất này đều là sản phẩm của quá trình điện phân NaCl có màng ngăn.
H2 + Cl2 → 2HCl (nhiệt độ)
|
GIÚP CON HỌC TOÁN KẾT HỢP VỚI TIẾNG ANH SIÊU TIẾT KIỆM CHỈ TRÊN MỘT APP MONKEY MATH. VỚI NỘI DUNG DẠY HỌC ĐA PHƯƠNG PHÁP GIÚP BÉ PHÁT TRIỂN TƯ DUY NÃO BỘ VÀ NGÔN NGỮ TOÀN DIỆN CHỈ VỚI 2K/NGÀY.
|
Ứng dụng của axit clohidric HCl
Với những tính chất vật lý và hóa học trên, axit clohidric HCl được ứng dụng như thế nào trong đời sống?
.jpg)
-
Trong công nghiệp: HCl 35% được sử dụng rộng rãi trong các ngành công nghiệp sắt thép, xi mạ, sản xuất chitin, luyện kim, hàn điện, sản xuất cao su, chế biến thực phẩm (đường, bột ngọt, nước mắm), công nghiệp hóa chất và xử lý nước, các nhà máy điện, công nghiệp khai thác khoáng sản…
-
Loại bỏ gỉ trên sắt thép: Đây là một ứng dụng đời sống thực tế và phổ biến nhất của axit HCl. Trước khi đưa thép vào sản xuất, người ta sẽ dùng HCl có nồng độ ~18% để tẩy gỉ các loại thép Carbon, khiến chúng trở nên mới. Bên cạnh đó, người ta đã phát minh quá trình tái chế HCl để tiết kiệm và nâng cao hiệu quả tẩy gỉ trên sắt thép theo phương trình:
4FeCl2 + 4H2O + O2 → 8 HCl + 2Fe2O3. Fe2O3 (sắt oxit) cũng là sản phẩm phụ được ứng dụng nhiều trong ngành công nghiệp.
-
Sử dụng sản xuất hợp chất vô cơ: Axit HCl được ứng dụng trong việc sản xuất các hợp chất vô cơ bằng nhiều phản ứng hóa học. Điển hình là các hóa chất xử lý nước như FeCl3, PAC,… được ứng dụng làm chất keo tụ, sử dụng trong xử lý nước thải, nước uống và sản xuất giấy.
-
Sản xuất hợp chất hữu cơ: HCl cũng có thể được dùng để tạo ra vinyl clorua và dicloroetan trong sản xuất PVC. Ngoài ra, nó cũng được ứng dụng trong sản xuất bisphenol A, sản xuất polycacbonat, axit ascobic, than hoạt tính và một số sản phẩm của ngành dược.
-
Kiểm soát, trung hòa độ pH: Trong các ngành công nghiệp yêu cầu độ tinh khiết (sản xuất dược phẩm, thực phẩm, dược phẩm, nước uống…), người ta sử dụng dung dịch HCl chất lượng cao để điều chỉnh nồng độ pH của nước. Với những ngành công nghiệp khác, axit clohydric HCL công nghiệp được sử dụng trung hòa nước thải và xử lý nước hồ bơi.
-
Tái sinh nhựa bằng cách trao đổi ion: HCL chất lượng cao được ứng dụng trong việc tái sinh nhựa trao đổi ion. Điều này được ứng dụng trong tất cả các ngành công nghiệp hóa, sản xuất đồ uống và một số ngành công nghiệp thực phẩm. HCL trở nên phổ biến nhằm loại bỏ các ion như Na+, Ca2+ từ dung dịch chứa nước tạo ra nước khử khoáng, thông qua sự thay thế Na+ bằng H+, Ca2+ bằng 2 H+.
-
Đối với sinh vật: Axit clohydric HCL có trong dạ dày với vai trò là một chất kháng lại các vi sinh vật, ngăn ngừa nhiễm trùng và hỗ trợ quá trình tiêu hóa. Khi nồng độ pH trong dạ dày thấp, các protein trong dạ dày bị biến tính, tạo điều kiện cho enzym tiêu hóa phân hủy thức ăn dễ dàng hơn, đồng thời kích hoạt các tiền enzym pepsinogen thành enzyme pepsin hoạt hóa nhờ sự tự phân cắt.
-
Các ứng dụng khác: Trong công nghiệp khai thác dầu, HCl được bơm vào trong tầng đá của giếng dầu để hòa tan một phần đá và tạo các lỗ rỗng lớn. HCl có khả năng hòa tan vàng và bạch kim khi trộn cùng axit nitric đậm đặc theo tỉ lệ mol 1:3. Axit clohidric cũng là thành phần sản xuất một số sản phẩm như: Aspartame, axit citric, lysine, fructose, thủy phân protein thực vật, gelatin….
Sơ lược về muối clorua
Muối của axit clohiđric HCl được gọi là muối clorua với công thức tổng quát: MCln. Vậy nên, nếu bạn băn khoăn HCL là muối hay bazơ thì có thể chắc chắn hơn đây là muối nhé.
.jpg)
-
Khả năng hòa tan: Các muối clorua hầu hết đều tan trong nước, trừ PbCl2, AgCl, CuCl và Hg2Cl2.
-
Ứng dụng: Muối clorua mang nhiều ứng dụng quan trọng như: Sử dụng làm phân kali (KCl), chống gỗ mục vì ZnCl2 có khả năng diệt khuẩn, làm chất xúc tác trong tổng hợp chất hữu cơ (AlCl3), diệt trừ sâu bệnh (BaCl2). NaCl là nguyên liệu quan trọng trong công nghiệp hóa chất điều chế hidro, clo và được sử dụng làm muối ăn và bảo quản thực phẩm.
-
Nhận biết: Để nhận biết muối clorua, ta sử dụng thuốc thử AgNO3 để tạo ra kết tủa trắng theo phương trình: AgNO3 + NaCl → AgCl + NaNO3.
Tổng hợp những phản ứng hóa học thường gặp nhất với HCl
Để ghi nhớ những kiến thức về hidro clorua, axit clohidric và muối clorua, sau đây là những phản ứng hóa học cơ bản và thường gặp nhất với HCl.
-
HCl phản ứng với kim loại
2HCl + Mg → MgCl2 + H2↑
Fe + 2HCl → FeCl2 + H2↑
6HCl + 2Al → 2AlCl3 + 3H2↑
Na + 2HCl → NaCl + H2↑
Zn + 2HCl → ZnCl2 + H2↑
-
HCl phản ứng với oxit kim loại
Fe3O4 + 8HCl → 4H2O + FeCl2+ 2FeCl3
6HCl + Al2O3 →2AlCl3 + 3H2O
MnO2 + HCl → MnCl2 + Cl2 + H2O
K2Cr2O7 + 14HCl → 2CrCl3 + 2KCl + 3Cl2 + 7H2O
KClO3 + 6HCl → 3Cl2 + KCl + 3H2O
-
HCl phản ứng với bazơ
2HCl + 2NaOH → 2NaCl + H2O
2HCl + Ca(OH)2 → CaCl2 + 2H2O
2HCl + Fe(OH)2 → FeCl2 + 2H2O
2HCl + Mg(OH)2 → MgCl2 + 2H2O
NH3 + HCl → NH4Cl (hiện tượng khói trắng bay ra)
-
HCl phản ứng với oxit bazơ
MgO + 2HCl → MgCl2 + H2O
2HCl + CuO → CuCl2 + H2O
-
HCl phản ứng với muối
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
K2CO3 + 2HCl → H2O + CO2 + 2KCl
AgNO3 + HCl → AgCl↓ + HNO3
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O

Monkey Math - Ứng dụng học toán tiếng Anh chỉ với 2K/Ngày
Nhóm halogen và tất tần tật thông tin chi tiết
Clo là gì? Khái niệm, tính chất, ứng dụng và cách điều chế
Bài tập về HCl SGK kèm lời giải chi tiết
Sau khi đã nắm chắc các kiến thức cơ bản về hidro clorua, axit clohidric và muối clorua, cùng tham khảo một số bài tập về HCl trong SGK Hóa 10 Bài 23. Hi vọng lời giải chi tiết, dễ hiểu nhất dưới đây sẽ giúp bạn đọc hiểu rõ hơn về bài học này.
.jpg)
Giải Bài 1 trang 106 SGK Hóa 10
Cho 20g hỗn hợp bột Mg và Fe tác dụng với dung dịch HCl dư thấy có 1g khí H2 bay ra. Khối lượng muối clorua tạo ra trong dung dịch là bao nhiêu gam?
A. 40,5g.
B. 45,5g.
C. 55,5g.
D. 65,5g.
Lời giải: Đáp án C đúng.
Ta có:
n(H2) = 1/2 = 0,5 mol.
Mg + 2HCl → MgCl2 + H2
Fe + 2HCl → FeCl2 + H2
n(Mg)= x; n(Fe) = y.
n(H2) = x + y = 0,5 mol.
mhh = 24x + 56y = 20g.
Giải hệ phương trình ta có x = y =0,25 mol.
mMgCl2 = 0, 25 × 95 = 23,75g.
mFeCl2 = 0,25 × 127 = 31,75g
Khối lượng muối clorua = 23,75 + 31,75= 55,5
Giải Bài 2 Hoá 10 SGK trang 106
Nêu những tính chất vật lí của khí hiđro clorua HCl.
Lời giải:
Hiđro clorua là chất khí không màu, mùi xốc, nặng hơn không khí. Khí hiđro clorua tan nhiều trong nước, tạo thành dung dịch axit. Ở 20oC, một thể tích nước có thể hòa tan 500 thể tích hiđro clorua.
Giải Bài 3 SGK Hóa 10 trang 106
Có các chất sau: Axit sunfuric đặc, nước, kali clorua rắn. Hãy viết các phương trình phản ứng để điều chế hidro clorua.
Lời giải:
Phương trình hóa học của phản ứng điều chế hidro clorua
2NaCl (tinh thể) + H2SO4 (đậm đặc) → Na2SO4 + 2HCl (nhiệt độ)
2KCl + 2H2O → 2KOH + H2 + Cl2 (điện phân dung dịch có màng ngăn)
H2 + Cl2 → 2HCl (ánh sáng)
Giải Bài 4 trang 106 SGK Hóa 10
Hãy dẫn ra những phản ứng hóa học của axit clohidric để làm thí dụ.
a) Đó là những phản ứng oxi hóa – khử.
b) Đó không phải là phản ứng oxi hóa – khử.
Lời giải:
a) Những ví dụ chứng minh axit clohidric là phản ứng oxi hóa – khử là:
Với vai trò là chất khử:
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
K2Cr2O7 + 14HCl --> 2CrCl3 + 2KCl + 3Cl2 + 7H2O
KClO3 + 6HCl --> 3Cl2 + KCl + 3H2O
Với vai trò là chất oxi hóa:
Mg + 2HCl → MgCl2 + H2↑
Mg + 2HCl → MgCl2 + H2↑
Fe + 2HCl → FeCl2 + H2↑
b) Những ví dụ không phải là phản ứng oxi hóa khử của axit clohidric:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
CuO + 2HCl → CuCl2 + H2O.
Giải Bài 5 Hoá 10 SGK trang 106
Bản chất của các phản ứng điều chế hiđro clorua bằng phương pháp sunfat và phương pháp tổng hợp khác nhau như thế nào? Các phương pháp trên đã dựa vào những tính chất hóa học nào của các chất tham gia phản ứng?
Lời giải:
Bản chất của phương pháp sunfat là dùng phản ứng trao đổi: NaCl + H2SO4 → NaHSO4 + HCl.
Bản chất của phương pháp tổng hợp là dùng phương pháp hóa hợp (phản ứng oxi hóa – khử):
H2 + Cl2 → 2HCl.
Bài tập về axit clohidric HCL để các em tự luyện
Ngoài những bài tập trong sách giáo khoa, dưới đây là một số bài tập thực hành mà Monkey tổng hợp để hỗ trợ việc học kiến thức HCL của các em tốt hơn:
Câu 1: Chất nào sau đây có tên gọi là hiđroclorua?
A. dd HCl. B. khí Cl2.
C. khí HCl. D. dd HClO.
Câu 2: Trộn dd chứa 1 g HCl vào dd chứa 1 g NaOH. Nhúng giấy quì tím vào dung dịch thu được thì giấy quì tím chuyển sang màu gì?
A. Màu đỏ. B. Màu xanh.
C. Không màu. D. Màu tím.
Câu 3: Số oxi hóa của Cl trong HCl là
A. +1. B. -1.
C. 0. D. -2.
Câu 4: Cho lượng dư dung dịch AgNO3 vào dung dịch hỗn hợp gồm 0,1 mol NaF và 0,1 mol NaCl. Khối lượng kết tủa tạo thành là
A. 14,35 g. B. 10,8 g.
C. 21,6 g. D. 27,05 g.
Câu 5: Cho 0,3 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 0,28 lít H2 (đktc). Kim loại đó là?
A. Ba B. Ca.
C. Mg. D. Sr.
Câu 6: Cho m gam hỗn hợp Zn, Fe tác dụng với vừa đủ với 73 g dd HCl 10%. Cô cạn dd thu được 13,15 g muối. Giá trị m là
A. 7,05 g. B. 5,3 g.
C. 4,3 g. D. 6,05 g.
Câu 7: Cho 15 gam hỗn hợp bột kim loại Zn và Cu vào dung dịch HCl dư, sau khi phản ứng xảy ra hoàn toàn thu được 4,48 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là
A. 6,4. B. 8,5.
C. 2,2. D. 2,0
Câu 8: Cho 17,4 gam MnO2 tác dụng với dd HCl đặc, dư và đun nóng. Thể tích khí thoát ra (đktc) là
A. 4,48 lít. B. 2,24 lít.
C. 3,36 lít. D. 6,72 lít.
Câu 9: Kim loại tác dụng được với axit HCl loãng và khí clo cho cùng một loại muối clorua kim loại là:
A. Fe. B. Zn.
C. Cu. D. Ag.
Câu 10: Cho 10,5g hỗn hợp bột Mg, Fe tác dụng với dung dịch HCl dư thấy có 0,4g khí H2 bay ra. Khối lượng muối thu được sau phản ứng là
A. 17,6g B. 25,1g
C. 24,7g D. 17,8g
Câu 11: Trong muối NaCl có lẫn NaBr và NaI. Để loại hai muối này ra khỏi NaCl người ta có thể
A. nung nóng hỗn hợp.
B. cho hỗn hợp tác dụng với dung dịch HCl đặc.
C. cho hỗn hợp tác dụng với Cl2 sau đó đun nóng.
D. cả A, B và C.
Câu 12: Hòa tan 12,8 gam hỗn hợp gồm Fe, FeO bằng dd HCl vừa đủ, thu được 2,24 lít (đktc). Thành phần phần trăm theo khối lượng của FeO trong hỗn hợp là
A. 56,25% B. 43,75%
C. 66,67% D. 33,33%
Câu 13: Trong các phản ứng sau, phản ứng nào sai?
A. Cu(OH)2 + 2HCl → CuCl2 + 2H2O.
B. Cu + 2HCl → CuCl2 + H2.
C. CuO + 2HCl → CuCl2 + H2O.
D. AgNO3 + HCl → AgCl + HNO3.
Câu 14: Để trung hoà 100 ml dung dịch NaOH 1,5M thì thể tích dung dịch HCl 0,5M cần dùng là bao nhiêu?
A. 0,5 lít. B. 0,4 lít.
C. 0,3 lít. D. 0,6 lít.
Câu 15: Đổ dung dịch AgNO3 vào dung dịch axit nào sau đây sẽ thu được kết tủa trắng?
A. HF B. HBr
C. HI D. HCl
Như vậy, bài viết này đã giúp bạn trả lời câu hỏi HCl là gì và cung cấp những kiến thức cơ bản quan trọng về hidro clorua, axit clohidric và muối clorua. Monkey mong rằng, những thông tin trên đây sẽ giúp bạn hiểu rõ hơn về HCL và có thể giải thành thạo các bài tập liên quan đến loại chất này trong tương lai. Ấn “NHẬN CẬP NHẬT” phần đầu trang để không bỏ lỡ những bài học thú vị khác nhé!
Hydrochloric acid - Ngày truy cập: 12/7/2022
https://en.wikipedia.org/wiki/Hydrochloric_acid
hydrogen chloride chemical compound - Ngày truy cập: 12/7/2022









.png)
.png)

![[Thảo luận] Giai đoạn chuyển tiếp ở trẻ | Kỷ luật tích cực #19](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:22:39_giai-doan-chuyen-tiep-o-tre-ky-luat-tich-cuc.png)
![[Thảo luận] Tác hại khi phạt trẻ bằng đòn roi | Kỷ luật tích cực #18](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:16:33_tac-hai-khi-phat-tre-bang-don-roi-ky-luat-tich-cuc.png)
![[Thảo luận] Cơn thịnh nộ (ăn vạ) của trẻ | Kỷ luật tích cực #17](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:04:28_con-thinh-no-va-an-va-cua-tre-ky-luat-tich-cuc.png)


.png)