Có tới 4.610.000 kết quả trong vòng 0,35 giây khi tìm kiếm từ khóa “tác hại của lưu huỳnh” trên google. Vậy lưu huỳnh là gì, có độc hay không? Cùng tìm hiểu tính chất đặc trưng và những ứng dụng phổ biến nhất của loại chất phổ biến này.
.png)
Lưu huỳnh là gì?
Lưu huỳnh (còn có tên khác là sulfur, lưu hoàng hay diêm sinh) là một nguyên tố hóa học nằm trong bảng tuần hoàn có ký hiệu S và số nguyên tử 16. Ngoài ra, đây còn là một phi kim phổ biến, không mùi, không vị, nhiều hóa trị. Dạng gốc của lưu huỳnh là chất rắn kết tinh màu vàng chanh, được xem là một nguyên tố thiết yếu cho sự sống và chúng được tìm thấy trong 2 axit amin.
Lưu huỳnh có ở đâu?
-
Trong tự nhiên, lưu huỳnh có thể được tìm thấy ở dạng đơn chất, trong các khoáng chất sulfua và sulfat.
-
Lưu huỳnh dạng đơn chất xuất hiện xung quanh các suối nước nóng, các khu vực núi lửa tại nhiều nơi trên thế giới, đặc biệt là khu vực dọc theo vành đai lửa Thái Bình Dương.
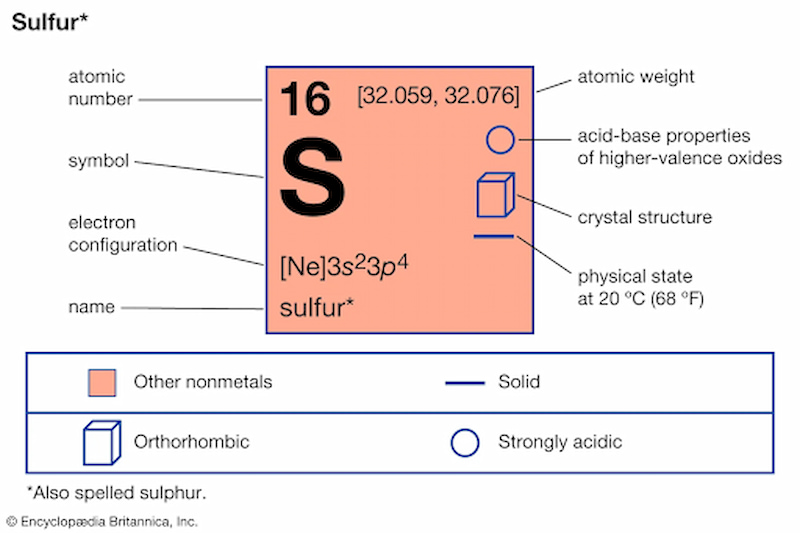
Số hiệu nguyên tử: 16
Vị trí: thuộc nhóm VIA, chu kì 3 trong bảng tuần hoàn các nguyên tố hóa học.
Cấu hình e: 1s22s22p63s23p4 với 6 e lớp ngoài cùng.
Những tính chất vật lý của lưu huỳnh
Lưu huỳnh mang những tính chất vật lý sau đây:

-
Trạng thái: Ở nhiệt độ phòng, lưu huỳnh là một chất rắn xốp có màu vàng nhạt. Lưu huỳnh trong trạng thái này thông thường tồn tại như các phân tử vòng dạng vòng hoa S8. Bên cạnh đó, nó còn mang nhiều hình thù khác. Loại một nguyên tử từ vòng sẽ là S7, đây chính là nguyên nhân cho màu vàng đặc trưng của nó. Ngoài ra, lưu huỳnh còn tồn tại ở dạng vô định hình, hay còn gọi là lưu huỳnh dẻo.
-
Tinh thể: Lưu huỳnh có tinh thể rất phức tạp, phụ thuộc vào các điều kiện khác nhau. Các dạng hình thù của chúng tạo thành các cấu trúc tinh thể khác nhau, có thể là các dạng hình thoi và xiên đơn S8 là các dạng tinh thể được nghiên cứu tỉ mỉ nhất.
-
Mùi: Lưu huỳnh không được ưa thích do mùi của nó khá giống với mùi trứng ung - đây là đặc trưng của hydro sulfide (H2S). Lưu huỳnh đơn chất không có mùi. Khi cháy, nó tạo ra ngọn lửa màu xanh lam và tỏa ra lưu huỳnh dioxide - một mùi ngột ngạt khác thường.
-
Khả năng hòa tan: Lưu huỳnh không hòa tan trong nước nhưng lại hòa tan được trong cacbon disulfide và các dung môi không phân cực khác.
-
Các mức oxi hóa: Lưu huỳnh có các mức oxi hóa là: -2, -1 (pirit sắt...), +2, +4, +6. Lưu huỳnh có khả năng tạo thành các hợp chất ổn định với hầu hết mọi nguyên tố, ngoại trừ các khí trơ.
-
Nóng chảy: Lưu huỳnh nóng chảy thường có độ nhớt, đây cũng là tính chất nổi bật của phi kim này. Độ nhớt của lưu huỳnh tăng lên theo nhiệt độ do sự hình thành các chuỗi polyme. Tuy nhiên, sau khi đạt được một khoảng nhiệt độ nhất định, độ nhớt lại bị giảm xuống vì đã đủ năng lượng cần thiết để phá vỡ chuỗi polymer.
Dạng hình thù của lưu huỳnh
Lưu huỳnh có hai dạng thù hình, là lưu huỳnh tà phương Sα và lưu huỳnh đơn tà Sβ. Hai dạng thù hình này khác nhau về cấu tạo tinh thể và một số tính chất vật lí, nhưng lại mang tính chất hóa học giống nhau. Hai dạng lưu huỳnh Sα và Sβ này có thể biến đổi qua lại với nhau tùy theo điều kiện nhiệt độ. Theo dõi bảng dưới đây để hiểu chi tiết sự biến đổi qua lại này:
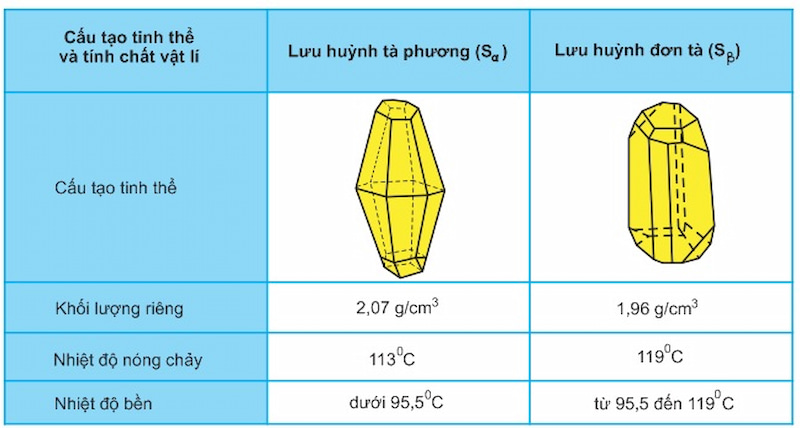
Ảnh hưởng của nhiệt độ đến tính chất vật lý của lưu huỳnh
Tính chất vật lý của lưu huỳnh có sự biến đổi rõ rệt theo nhiệt độ khác nhau. Cụ thể là:
-
Ở nhiệt độ dưới 113 độ: Sα và Sβ đều là chất rắn màu vàng. Trong phân tử có 8 nguyên tử liên kết cộng hóa trị với nhau tạo mạch vòng.
-
Ở nhiệt độ 119 độ: Sα và Sβ nóng chảy thành chất lỏng màu vàng và rất linh động.
-
Ở nhiệt độ 187 độ: Lưu huỳnh lỏng ở trạng thái quánh nhớt và có màu nâu đỏ.
-
Ở nhiệt độ 445 độ: Lưu huỳnh sôi, các phân tử lưu huỳnh bị phá vỡ thành nhiều phân tử nhỏ bay hơi.
Ví dụ: 1400 độ C, hơi lưu huỳnh là những phân tử S2. Nhưng ở 1700 độ C, lưu huỳnh là những nguyên tử S.
Tính chất hóa học của lưu huỳnh
Điểm nổi bật trong tính chất hóa học của lưu hình là nó vừa thể hiện tính oxi hóa với các mức oxi hóa khác nhau, bao gồm: -2, 0, +4, +6, lại vừa thể hiện tính khử. Cùng tìm hiểu chi tiết tính chất này trong các thí nghiệm lưu huỳnh tác dụng với kim loại, Hidro và phi kim.

Tính chất của lưu huỳnh khi tác dụng với kim loại và Hidro
Ở nhiệt độ cao, lưu huỳnh tác dụng với Hidro tạo ra khí hidro sunfua và tác dụng với kim loại tạo ra muối sunfua.
Tác dụng với hidro
Khi dẫn khí H2 vào ống thí nghiệm đựng lưu huỳnh đang sôi, lưu huỳnh phản ứng hóa học trực tiếp với Hidro. Quan sát thí nghiệm, ta nhận thấy có khí mùi trứng thối xuất hiện, đó là hiđro sunfua.
Phương trình phản ứng: H2 + S →H2S (điều kiện nhiệt độ: 350 độ)
Tác dụng với kim loại
Tác dụng với kim loại là một trong những tính chất hóa học đặc trưng của lưu huỳnh. Khi đun nóng, lưu huỳnh có khả năng tác dụng với nhiều kim loại tạo ra nhiều hợp chất khác nhau.
Ví dụ:
-
Khi trộn hỗn hợp bột sắt và lưu huỳnh, sau đó đun nhẹ. Quan sát phản ứng, ta thấy phản ứng tỏa nhiều nhiệt và xảy ra mạnh hơn theo phương trình: FE + S → FeS (điều kiện nhiệt độ)
-
Lưu huỳnh tác dụng với kẽm và nhôm cũng xảy ra phản ứng mạnh kèm theo sự lóe sáng. Những sợi đồng mảnh có thể cháy trong lưu huỳnh tạo ra CuS có màu đen.
Một điểm đáng chú ý là thủy ngân phản ứng với lưu huỳnh ở ngay nhiệt độ thường theo phương trình: Hg + S → HgS. Trong phản ứng này, S thể hiện tính oxi hóa, nó oxi hóa Fe (0), Hg (0) thành Fe(+2) và Hg(+02), oxi hóa H(0) thành H(1).
Tác dụng với phi kim
Ở nhiệt độ thường, lưu huỳnh tác dụng với hầu hết các nguyên tố phi kim mạnh hơn như flo, oxi, clo… trừ iot và nitơ. Khi đốt cháy lưu huỳnh trong trong không khí ta được lưu huỳnh (IV) oxit với ngọn lửa màu xanh.
S + O2 → SO2 (nhiệt độ)
S + 3F2 → SF6 (nhiệt độ)
Trong các phản ứng này, lưu huỳnh thể hiện tính khử của mình khi khử O(0) thành O(-2), khử F(0) thành F(-1).
Điều chế lưu huỳnh như thế nào?
Ở phần này, chúng ta cùng tìm hiểu hai cách điều chế lưu huỳnh theo hai phương pháp phổ biến hiện nay: Trong phòng thí nghiệm và điều chế trong công nghiệp.
Trong phòng thí nghiệm
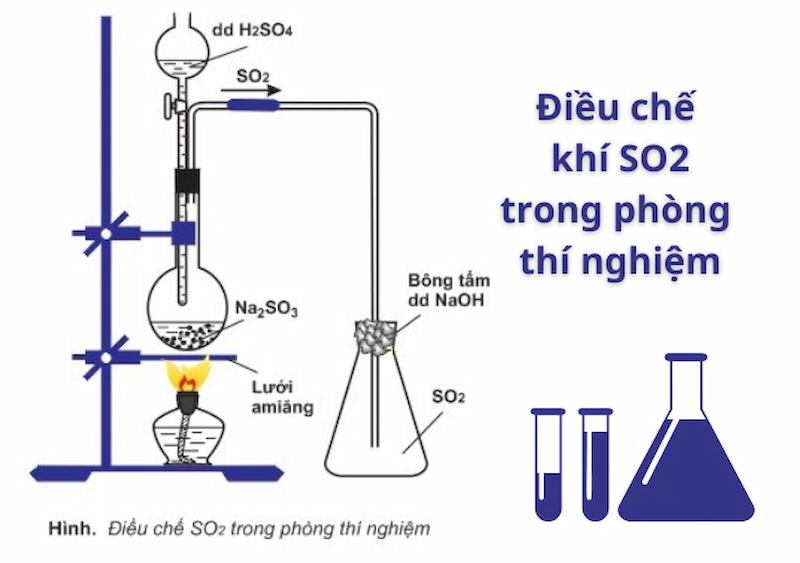
Trong phòng thí nghiệm, lưu huỳnh được điều chế bằng cách: Cho muối sunfit (muối của axit yếu) tác dụng với axit mạnh hơn (thường là dung dịch axit sunfuric với muối natri sunfit) theo quy trình sau:
-
Rót từ từ dung dịch axit sunfuric vào bình có chứa natri sunfit, sau đó đậy nắp lại theo phương trình: H2SO4 + Na2SO3 → Na2SO4 + SO2 + H2O (điều kiện: đun nóng). Chú ý cần để bình thu khí dựng thẳng, vì SO2 nặng hơn không khí.
-
Đun nóng bình trên ngọn lửa đèn cồn và sử dụng lưới amiang. Loại lưới này có tác dụng chống không cho ngọn lửa tập trung tại một chỗ và làm vỡ bình khi đun nóng dung dịch
-
Khí lưu huỳnh dioxit được thu lại bằng phương pháp chuyển không khí. Người ta dùng bông tẩm dung dịch natri hidroxit (NaOH) để hạn chế lượng khí SO2 thoát ra.
Chú ý:
-
Không dùng bông tẩm khí amoniac (NH3) vì đây là khí dễ bay hơi khiến việc thu khí kém đạt hiệu quả.
-
Cho muối sunfit tác dụng với axit clohidric tránh trường hợp axit này bay hơi và hòa lẫn vào SO2, ảnh hưởng đến kết quả chính xác.
Trong công nghiệp
Trong công nghiệp, lưu huỳnh được điều chế bằng những phương pháp phổ biến sau:
-
Đốt lưu huỳnh: S + O2 (nhiệt độ) → SO2
-
Đốt cháy H2S trong oxi dư: 2H2S + 3O2 → 2H2O + 2SO2
-
Cho kim loại tác dụng với H2SO4 (đặc nóng): Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
-
Đốt quặng pirit sắt (FeS2): 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
|
XÂY DỰNG NỀN TẢNG TOÁN HỌC VỮNG CHẮC CHO TRẺ TỪ NHỎ VỚI ĐA PHƯƠNG PHÁP DẠY HỌC TÍCH CỰC, CHI PHÍ CỰC RẺ CHƯA ĐẾN 2K/NGÀY CÙNG MONKEY MATH.
|
Những ứng dụng quan trọng của lưu huỳnh trong công nghiệp và đời sống
Lưu huỳnh là một trong những nguyên tố liên quan đến nhiều lĩnh vực trong đời sống thực tiễn, góp vai trò quan trọng trong nền kinh tế thế giới.
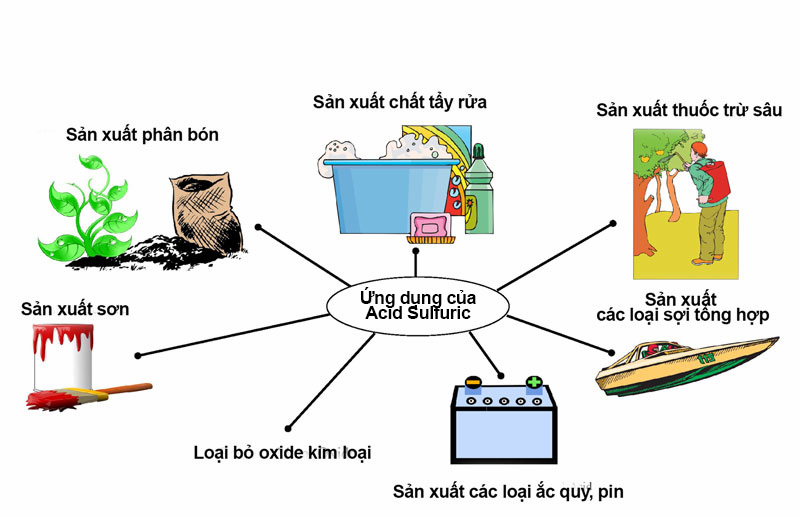
Bột lưu huỳnh có tác dụng gì trong công nghiệp
Trong công nghiệp, 90% lượng lưu huỳnh được khai thác thông qua dẫn xuất chính là axít sulfuric (H2SO4), đây được đánh giá là một trong các nguyên tố quan trọng nhất được sử dụng như một nguyên liệu công nghiệp.
Việc tiêu thụ acid sulfuric còn được coi là một trong các chỉ số tốt nhất về sự phát triển công nghiệp của một quốc gia. Lưu huỳnh được sản xuất ở Hoa Kỳ hàng năm nhiều hơn bất kỳ hóa chất công nghiệp nào khác.

Lưu huỳnh được sử dụng trong nhiều sản phẩm công nghiệp, ví dụ như: Ắc quy, bột giặt, lưu hóa cao su, thuốc diệt nấm và các phân bón photphat. Cụ thể, được lưu huỳnh được sử dụng để tạo nên độ trắng của giấy, làm chất bảo quản trong rượu vang và làm khô hoa quả. Do bản chất dễ cháy, lưu huỳnh còn được ứng dụng trong sản xuất các loại diêm, thuốc súng, thuốc nổ cũng như pháo hoa…
Ứng dụng của lưu huỳnh trong làm đẹp
Từ xa xưa, con người đã biết ứng dụng lưu huỳnh trong việc làm đẹp da và trị mụn trứng cá. Tuy nhiên, hiện nay vẫn chưa có nghiên cứu rõ ràng nào tìm ra cách hoạt động của nguyên tố này trong việc điều trị mụn.
Qua thực nghiệm, người ta đưa ra kết luận: Lưu huỳnh có khả năng kháng viêm và kháng khuẩn cao, từ đó có khả năng khiến những nốt mụn xẹp đi một cách nhanh chóng.

Ứng dụng của lưu huỳnh trong nông nghiệp
Bên cạnh những ứng dụng quan trọng bậc nhất của ngành công nghiệp, trong lĩnh vực nông nghiệp, lưu huỳnh cũng được xem như một trong những nguyên liệu để chế tạo phân bón hóa học, thuốc trừ sâu, thuốc diệt nấm…
Ứng dụng lưu huỳnh trong y học
Lưu huỳnh cũng thể hiện vai trò của mình trong y học. Magnesi sulfat có thể được sử dụng như một loại thuốc nhuận tràng và điều trị các bệnh liên quan đến rối loạn về da với tính năng kháng viêm, kháng khuẩn cao.
Ví dụ: Kem, sữa dưỡng da, thuốc mỡ hoặc xà phòng lưu huỳnh dùng điều trị mụn trứng cá, thuốc mỡ lưu huỳnh dùng để điều trị viêm da tiết bã, ghẻ…
Xem thêm:
- Nhóm halogen là gì? Vị trí, đặc điểm, tính chất, cấu hình electron
- Iot là gì? Tính chất và những ứng dụng phổ biến nhất
Lưu huỳnh có độc không? Những ảnh hưởng tiêu cực của lưu huỳnh đến môi trường và con người
Khi tìm kiếm các thông tin liên quan đến “tác hại của lưu huỳnh” trên Google, người dùng có được 4.610.000 kết quả chỉ trong 0,35 giây. Vậy lưu huỳnh có thật sự độc không, và tác hại của nó là gì?

Lưu huỳnh có độc không?
Lưu huỳnh là một nguyên tố hóa học độc hại nếu sử dụng với hàm lượng lớn. Mặc dù lưu huỳnh dioxide khá an toàn khi được sử dụng một lượng nhỏ, nhưng khi ở nồng độ cao với một liều lượng đủ lớn, nó phản ứng với hơi ẩm để tạo ra axit sulfuro có thể gây tổn thương cho phổi, mắt hay các cơ quan khác.
Những ảnh hưởng tiêu cực của lưu huỳnh
Lưu huỳnh công nghiệp là hóa chất độc hại không được phép sử dụng trong chế biến và bảo quản thực phẩm. Tuy nhiên ở nước ta, vì yếu tố lợi nhuận, tình trạng lạm dụng lưu huỳnh công nghiệp rất phổ biến trong bảo quản tẩm sấy các dược liệu… gây tác động tiêu cực tới sức khỏe con người, môi trường cùng các loại sinh vật sống.
Tác động đến sức khỏe con người
Theo khuyến cáo của Tổ chức Y tế thế giới (WHO), hàm lượng SO2 có trong các loại thực phẩm không được vượt quá 20mg/1kg. Nhưng nhưng ở Việt Nam, lượng lưu huỳnh được sử dụng cao hơn rất nhiều lần so với mức độ cho phép. Không chỉ ảnh hưởng đến cơ thể qua đường tiêu hóa, lưu huỳnh còn gây hại cho con người thông qua việc ngửi chúng.
Khi ngửi mùi lưu huỳnh quá nhiều hoặc tiếp xúc trực tiếp với khí lưu huỳnh khi cháy sẽ gây ra các vấn đề về sức khỏe. Điển hình là:
-
Đau đầu: SO2 sẽ xâm nhập vào cơ thể sau đó ngấm vào máu và làm ảnh hưởng đến hệ thần kinh khi con người hít phải chúng. Chính vì vậy, ngay khi ngửi phải mùi của lưu huỳnh, bạn sẽ thấy đau đầu, tùy theo nồng độ mùi.
-
Ngạt mũi: Lưu huỳnh cháy sản sinh khí lưu huỳnh đioxit (SO2) cùng các hạt bụi li ti sẽ khiến người hít phải ngạt mũi, ảnh hưởng trực tiếp đến sự thở tùy theo nồng độ.
-
Khó thở: SO2 đi vào trong cơ thể sẽ làm giảm dự trữ lượng kiềm trong máu gây rối loạn chuyển hoá đường và protein, gây thiếu vitamin B và C, tắc nghẽn mạch máu. Điều này khiến người hít phải lưu huỳnh bị co hẹp dây thanh quản, khó thở.
-
Viêm phế quản: Lưu huỳnh thâm nhập vào cơ thể qua mũi hoặc miệng sẽ hòa tan với các hạt nước nhỏ hoặc bụi ẩm và tạo thành các hạt axit sunfuric (H2SO4). Sau đó, chúng xâm nhập qua phổi và gây ra những bệnh lý về phổi khác nhau trong đó có viêm phế quản.
-
Ngộ độc máu: SO2 xâm nhập cơ thể làm tăng lượng axit và giảm kiềm, từ đó gây ngộ độc máu.
-
Tử vong: Khi lưu huỳnh đi vào cơ thể ở nồng độ cao, máu bị ngộ độc, hệ thần kinh bị tác động, phổi bị ảnh hưởng…. từ đó khiến các cơ quan quan trọng tê liệt, có thể dẫn đến tử vong.
Như vậy, khi tiếp xúc trực tiếp với lưu huỳnh qua đường ngửi hay ăn uống, con người đều phải đối mặt với nhiều vấn đề về sức khỏe nghiêm trọng tùy theo mức độ. Do đó, khi tiếp xúc với lưu huỳnh, bạn không nên tiếp xúc trực tiếp. Đối với những thực phẩm có tẩm lưu huỳnh, hãy rửa thật sạch với nước trước khi chế biến, sử dụng.
Tác động đến sinh vật dưới nước
Khi nguồn nước bị nhiễm lưu huỳnh công nghiệp, các sinh vật và vi sinh vật sống dưới nước có thể bị ảnh hưởng nghiêm trọng. Điển hình như cá, tôm, cua, ngao, sò,... chúng sẽ bị ngộ độc lưu huỳnh và chết hàng loạt. Nguy hiểm hơn, khi ăn phải các loại sinh vật này, con người cũng có nguy cơ rất cao bị nhiễm độc lưu huỳnh gián tiếp.
Tác động đến môi trường sống
Khi đốt lưu huỳnh ở nhiệt độ cao, môi trường sống sẽ bị hủy hoại nghiêm trọng, gây ô nhiễm môi trường khí, biến đổi khí hậu, mưa axit, hiệu ứng nhà kính…
-
Ô nhiễm môi trường: Lưu huỳnh đioxit là tác nhân gây ô nhiễm môi trường.
-
Mưa axit: SO2 bị oxy hóa và khi tác dụng với nước hình thành axit sunfuric tạo ra mưa axit - gây tổn thương cho các loài thực vật (khi tiếp xúc với môi trường chứa SO2 1- 2 ppm trong vài giờ).
-
Phá hủy tầng ozon: SO2 + O3 → SO3 + O2
-
Ô nhiễm nguồn nước: Hydrogen sulfide (H2S) - một loại khí được hình thành do sự phân hủy các chất hữu cơ là một trong những nguyên nhân gây ô nhiễm nguồn nước, chất này thường được tìm thấy chủ yếu trong nước giếng khoan. Khi nước chứa hàm lượng H2S thấp khoảng 1,0 PPM sẽ có đặc tính ăn mòn. Lúc này, nó trở thành axit gây ăn mòn kim loại, bê tông và khiến thay đổi tính chất vật lý, màu sắc của đá vôi, đá hoa, phá hủy kiến trúc, gây gỉ sét cho sắt, thép, bào mòn và khiến vải sợi, giấy xuất hiện chấm đen…

Monkey Math - Ứng dụng học toán tiếng Anh chỉ với 2K/Ngày

Oxi: Tính chất, ứng dụng và cách điều chế [Tổng hợp Lớp 8 + 10]

Hóa trị là gì? Quy tắc hóa trị bạn cần nhớ và cách vận dụng
Lưu ý khi sử dụng và cách lưu trữ, bảo quản lưu huỳnh
Vì tính chất độc hại của nó, khi sử dụng lưu huỳnh, bạn cần lưu ý những yếu tố sau đây để tránh gây ra những tác hại trực tiếp với sức khỏe cũng như môi trường sống.
Sử dụng lưu huỳnh cần lưu ý những gì?
-
Đối với các hợp chất của lưu huỳnh, bạn cần thận trọng khi tiếp xúc với các hợp chất này (chẳng hạn như carbon disulfide, carbonyl sulfide, hydro sulfide và lưu huỳnh dioxide).
-
Khi sử dụng thuốc lưu huỳnh, bạn cần chú ý tới liều lượng dùng thuốc lưu huỳnh, thời gian sử dụng, hướng dẫn sử dụng và nghe theo sự chỉ định của bác sĩ chuyên môn.
Cách lưu trữ và bảo quản lưu huỳnh
-
Đối với hóa chất lưu huỳnh, bạn cần bảo quản nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp của mặt trời chiếu vào.
-
Đối với thuốc lưu huỳnh, bạn cần bảo quản ở nhiệt độ phòng, tránh nơi ẩm ướt và tránh ánh nắng mặt trời, tuyệt đối không bảo quản lưu huỳnh trong phòng tắm hoặc ngăn đá. Với thuốc hết hạn sử dụng, đừng tự ý vứt thuốc lưu huỳnh vào toilet hoặc đường ống dẫn nước, hãy tham khảo ý kiến của dược sĩ hoặc công ty xử lý rác thải địa phương để có cách tiêu hủy thuốc an toàn.
Một số hợp chất phổ biến của lưu huỳnh
Ở phần này, chúng ta cùng tìm hiểu một số hợp chất phổ biến của lưu huỳnh và đồng vị của nó.

Sulfua Hydro: Hợp chất chính của lưu huỳnh là Sunfua Hydro, có mùi trứng thối đặc trưng. Khi hoà tan trong nước, hợp chất này có tính axit và phản ứng với nhiều kim loại để tạo ra các sunfua kim loại. Các sunfua kim loại này khá phổ biến, nhất là của sắt (còn được gọi là pyrit).
Êtyl và mêtyl mecaptan: Hợp chất khác của lưu huỳnh như êtyl và mêtyl mecaptan có mùi khó ngửi và được sử dụng làm chất tạo mùi cho khí đốt nhằm phát hiện rò rỉ.
Nitrua lưu huỳnh polyme hóa: Được tạo ra từ têtranitrua têtra lưu huỳnh S4N4 - một hợp chất có các tính chất của kim loại mặc dù không chứa bất kỳ nguyên tử kim loại nào. Chúng có các tính chất quang học và điện bất thường và polyme này có thể tạo ra từ têtranitrua têtra lưu huỳnh S4N4.
Bên cạnh đó, một số hợp chất quan trọng khác của lưu huỳnh có thể kể đến như:
Một số hợp chất vô cơ:
-
Sulfua (S2-)
-
Sulfit (SO32-), các muối của axit sulfurơ, H2SO3, axít sulfurơ và các sulfit tương ứng, ion pyrosulfit, mêtabisulfit (S2O52−).
-
Sulfat (SO42-) và các muối của axit sulfuric.
-
Thiôsulfat (đôi khi được gọi là thiôsulfit hay “hyposulfit”) (S2O32−)- như thiôsulfat natri.
-
Đithiônit natri, Na2S2O4 tạo ra từ axít hyposulfurơ/đithiônơ.
-
Đithiônat natri (Na2S2O6)
-
Axit polythiônic (H2SnO6)
-
Axít perôxymônôsulfuric (H2SO5) và axít perôxyđisulfuric (H2S2O8)-
-
Polisulfua natri (Na2Sx)
-
Hexaflorua lưu huỳnh, SF6
-
Têtranitrua têtra lưu huỳnh S4N4
Một số hợp chất hữu cơ:
-
Đimêtyl sulfôniôprôpiônat (DMSP; (CH3)2S+CH2CH2COO-)
-
Thiol (hay mecaptan)
-
Thiolat
-
Sulfôxít
-
Sulfon
-
Thuốc thử Lawesson
-
Naptalen-1,8-điyl 1,3,2,4-đithiađiphốtphetan 2,4-đisulfua
Đồng vị: Lưu huỳnh có tất cả 18 đồng vị trong đó có 4 đồng vị ổn định: S32 (95,02%), S33 (0,75%), S34 (4,21%) và S36 (0,02%).
Bài tập về lưu huỳnh SGK Hóa học 10 kèm lời giải
Những bài tập về lưu huỳnh SGK Hóa lớp 10 được trình bày chi tiết, dễ hiểu nhất dưới đây sẽ giúp bạn hiểu rõ hơn về lưu huỳnh cùng những tính chất đặc trưng của nó.
Bài tập 1 trang 132 SGK Hóa 10
Lưu huỳnh tác dụng với axit sunfuric đặc, nóng:
S + 2H2SO4 → 3SO2 + 2H2O
Trong phản ứng này, tỉ lệ số nguyên tử lưu huỳnh bị khử: Số nguyên tử lưu huỳnh bị oxi hóa là:
A. 1 : 2.
B. 1 : 3.
C. 3 : 1.
D. 2 : 1.
Chọn đáp án đúng.
Gợi ý đáp án: D là đáp án đúng.
S là chất khử (chất bị oxi hóa) ⇒ Số nguyên tử S bị oxi hóa là 1
H2SO4 là chất oxi hóa (chất bị khử) ⇒ Số nguyên tử S bị khử là 2
→ Tỉ lệ số nguyên tử S bị khử: số nguyên tử S bị oxi hóa là: 2:1
Bài tập 2 Hoá 10 SGK trang 132
Dãy đơn chất nào sau đây vừa có tính oxi hóa vừa có tính khử?
A. Cl2 , O3, S.
B. S, Cl2, Br2.
C. Na, F2, S.
D. Br2, O2, Ca.
Gợi ý đáp án: B là đáp án đúng
Bài tập 3 SGK Hóa 10 trang 132
Có thể dự đoán sự thay đổi như thế nào về khối lượng riêng, về nhiệt độ nóng chảy khi giữ lưu huỳnh đơn tà (SB) dài ngày ở nhiệt độ phòng?
Gợi ý đáp án:
Ở nhiệt độ phòng, có sự chuyển hóa từ Sβ → Sα vậy khi giữ Sβ vài ngày ở nhiệt độ phòng thì:
-
Khối lượng riêng của lưu huỳnh tăng dần.
-
Nhiệt độ nóng chảy của lưu huỳnh giảm dần.
Bài tập 4 trang 132 SGK Hóa 10
Đun nóng một hỗn hợp gồm có 0,650g bột kẽm và 0,224g bột lưu huỳnh trong ống nghiệm đậy kín không có không khí. Sau phản ứng, người ta thu được chất nào trong ống nghiệm? Khối lượng là bao nhiêu?
Gợi ý đáp án:
n(Zn) = 0,65/65 = 0,01mol
n(s)= 0,224/32 = 0,007 mol
—> S phản ứng hết, Zn phản ứng dư
Phương trình hóa học của phản ứng
Zn + S → ZnS (nhiệt độ)
nZn phản ứng = 0,007 mol ⇒ nZnS = 0,007 mol.
Khối lượng các chất sau phản ứng:
mZn dư = (0,01 – 0,007) × 65 = 0,195g.
mZnS = 0,007 × 97 = 0,679g.
Bài tập 5 Hoá 10 SGK trang 132
1,10g hỗn hợp bột sắt và bột nhôm tác dụng vừa đủ với 1,28g bột lưu huỳnh.
a) Viết các phương trình hóa học của phản ứng xảy ra.
b) Tính tỉ lệ phần trăm của sắt và nhôm trong hỗn hợp ban đầu, theo:
-
Lượng chất.
-
Khối lượng chất.
Gợi ý đáp án:
a) Phương trình hóa học của phản ứng
Fe + S → FeS
2Al + 3S → Al2S3
b) Gọi nFe = x mol, theo PT ⇒ nS (1) = nFe = x mol
Gọi nAl = y mol, theo PT ⇒ nS (2) = (3/2). nAl = (3/2). y mol
⇒ nS = x + (3/2). y = 0,04 mol.
mhh = 56x + 27y = 1,1.
Giải hệ phương trình ta có x = 0,01 mol, y= 0,02 mol.
Tỉ lệ % sắt và nhôm trong hỗn hợp theo lượng chất ( theo số mol là):
%n(Fe) = x/(x+y). 100% = 30%
%n(Al) = 70%
Tỉ lệ phần trăm của sắt và nhôm trong hỗn hợp theo khối lượng chất:
mAl = 0,02 x 27 = 0,54g
mFe = 0,01 x 56 = 0,56g.
%mAl = (0.54/11)× 100% = 49,09%
%mFe = 100% - 49,09% = 50,91%
Bài tập về lưu huỳnh từ cơ bản để nâng cao để học sinh luyện tập
Ngoài bài tập trong sách giáo khoa hóa học 10, sau đây là một số bài tập mà Monkey tổng hợp để các em cùng nhau luyện tập:
Câu 1: Vị trí của nguyên tố lưu huỳnh (z = 16) trong bảng tuần hoàn hóa học là:
A. Ô thứ 16, chu kì 3, nhóm VIA.
B. Ô thứ 16, chu kì 2, nhóm VIA.
C. Ô thứ 16, chu kì 3, nhóm IVA.
D. Ô thứ 16, chu kì 2, nhóm IVA.
Câu 2: Nguyên tử nguyên tố X có tổng số electron ở các phân lớp p là 10. Nguyên tố X là
A. Na. B. Cl.
C. O. D. S.
Câu 3: Số oxi hóa có thể có của lưu huỳnh trong hợp chất là
A. 0, 2, 4, 6. B. -2, 0, +4, +6.
C. 1, 3, 5, 7. D. -2, +4, +6.
Câu 4: Lưu huỳnh thể hiện tính oxi hóa khi tác dụng với chất nào dưới đây?
A. O2. B. Al.
C. H2SO4 đặc. D. F2.
Câu 5: Cho phản ứng: S + 2H2SO4(đặc) → 3SO2↑ + 2H2O. Tỉ lệ số nguyên tử S bị khử và số nguyên tử S bị oxi hóa là
A. 1 : 2. B. 1 : 3.
C. 3 : 1. D. 2 : 1.
Câu 6: Có bao nhiêu gam SO2 hình thành khi cho 1,28 gam S phản ứng hoàn toàn với lượng O2 dư?
A. 2,28 g B. 2,00 g
C. 1,00 g D. 2,56 g
Câu 7: Đơn chất vừa có tính oxi hóa vừa có tính khử là
A. F2. B. O3.
C. S. D. O2.
Câu 8: Câu nào sau đây đúng khi nói về tính chất hoá học của lưu huỳnh?
A. Lưu huỳnh không có tính oxi hoá, tính khử.
B. Lưu huỳnh chỉ có tính oxi hoá.
C. Lưu huỳnh vừa có tính oxi hoá, vừa có tính khử.
D. Lưu huỳnh chỉ có tính khử.
Câu 9: Dãy gồm các chất đều tác dụng trực tiếp với lưu huỳnh là
A. Hg, O2, HCl.
B. Pt, Cl2, HCl.
C. Zn, O2, F2.
D. Na, Br2, H2SO4 loãng.
Câu 10: Kim loại nào sau đây tác dụng với lưu huỳnh ở nhiệt độ thường?
A. Al. B. Fe.
C. Hg. D. Cu.
Câu 11: Nhận định nào sau đây là sai?
A. S vừa có tính oxi hoá vừa có tính khử.
B. Hg phản ứng với S ngay nhiệt độ thường.
C. Ở nhiệt độ thích hợp, S tác dụng với O2, Cl2, F2 thể hiện tính oxi hóa.
D. Ở nhiệt độ cao, S tác dụng với nhiều kim loại và thể hiện tính oxi hoá.
Câu 12: Đun nóng 11,2 gam Fe trong lưu huỳnh dư, khối lượng muối thu được sau phản ứng là
A. 8,8g. B. 17,6g.
C. 4,4g. D. 35,2 g.
Câu 13: Cho 1,3 gam kẽm tác dụng với 0,32 gam lưu huỳnh. Sau khi phản ứng xảy ra hoàn toàn, sản phẩm thu được là
A. ZnS. B. ZnS và S.
C. ZnS và Zn. D. ZnS, Zn và S.
Câu 14: Nhận định nào sau về lưu huỳnh là sai?
A. S là chất rắn màu vàng.
B. S không tan trong nước.
C. S dẫn điện, dẫn nhiệt kém.
D. S không tan trong các dung môi hữu cơ.
Câu 15: Nung 6,5 gam Zn với bột lưu huỳnh. Khối lượng lưu huỳnh cần dùng để phản ứng hết với lượng kẽm là
A. 3,2 B. 1,6
C. 6,4 D. 4
Vậy lưu huỳnh là gì, lưu huỳnh có độc không, có những tính chất nào? Chắc hẳn qua bài viết trên đây của Monkey, bạn đã có câu trả lời chi tiết và rõ ràng nhất. Hy vọng bài viết này sẽ giúp ích bạn trong quá trình học tập của bản thân. Truy cập website của Monkey để có thêm nhiều thông tin về các nguyên tố Hóa học thú vị khác!
Sulfur - Ngày truy cập: 15/06/2022
https://en.wikipedia.org/wiki/Sulfur
Sulfur - Element information, properties and uses - Ngày truy cập: 15/06/2022










.png)
.png)

![[Thảo luận] Giai đoạn chuyển tiếp ở trẻ | Kỷ luật tích cực #19](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:22:39_giai-doan-chuyen-tiep-o-tre-ky-luat-tich-cuc.png)
![[Thảo luận] Tác hại khi phạt trẻ bằng đòn roi | Kỷ luật tích cực #18](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:16:33_tac-hai-khi-phat-tre-bang-don-roi-ky-luat-tich-cuc.png)
![[Thảo luận] Cơn thịnh nộ (ăn vạ) của trẻ | Kỷ luật tích cực #17](https://vnmedia2.monkeyuni.net/upload/web/storage_web/09-04-2026_12:04:28_con-thinh-no-va-an-va-cua-tre-ky-luat-tich-cuc.png)


.png)